重症筋無力症の経過・予後
2026年2月掲載
(審J2601241)
九州大学病院 脳神経内科
助教 渡邉 充 先生
【専門領域】
神経内科学、神経免疫学(MG, MS, NMOSD)
【所属学会】
日本内科学会、日本神経学会、日本神経免疫学会、日本臨床免疫学会、日本神経感染症学会、日本末梢神経学会、日本神経治療学会、日本認知症学会
【学会関連】
多発性硬化症・視神経脊髄炎スペクトラム障害診療ガイドライン2023:システマティックレビュー委員
HTLV-1関連脊髄症(HAM)診療ガイドライン2025:研究協力者
重症筋無力症(myasthenia
gravis:MG)は慢性疾患で、多くの場合、MG症状は生涯にわたって経過する。しかし近年は、診断技術の向上、免疫療法の普及といった診療の進歩により、死亡例や重症例は減少し、症状の改善が得られる患者の割合は増加している。ここでは、MGの経過と予後について概説する。
MGの病型別分類と眼筋型MGの臨床経過
MGの病型は、眼瞼下垂や複視などの眼症状に限定される眼筋型MGと、四肢や呼吸筋などの全身の筋力低下や易疲労性を認める全身型MGの2つに大別される。MG患者の約半数は眼筋型MGとして発症するが1,2)、その経過には特徴がある。
眼筋型MGでは発症から1年以内に症状が最も強くなることが多く、この時期にピークを迎える患者は約70%にのぼる3)。一方で、約20%の患者は発症から6ヵ月以内に寛解すると報告されている3)。
また、近年のメタ解析で眼筋型MGの39%が全身型へ進展するとされているが、報告によって11~84%と様々である4)。Hendricksらによると、眼筋型MGが全身型MGへ移行するまでの中央値は13ヵ月であり5)、1年以上経過してから進展する症例は12%にとどまる3)。さらに、Bever
CT
Jrらの後ろ向き研究では、発症時に眼症状のみを呈した患者のうち、眼症状のまま2年以上経過した後に全身型へ進展した症例は15%にすぎず、大多数は2年以内に全身型へ移行していたと報告されている6)。
なお、全身型MGへの進展リスクを高める因子として、女性であること(男性より6%リスクが高い)や診断時の抗アセチルコリン受容体抗体(抗AChR抗体)陽性(陰性群より30%リスクが高い)が挙げられている4)。一部の研究では単線維筋電図(SFEMG)異常が挙げられており、5年時点での全身化率はそれぞれ、抗AChR抗体陽性例で67%(陰性例では11%)、SFEMG異常例では77%(正常例では18%)と報告されている5)。
全身型MGの経過と長期予後の変遷
全身型MGの経過も眼筋型MGと同様に、発症から最初の1年間に症状が増悪しやすい3)。1966~2000年の米国における全身型MG患者980例を対象としたGrob
Dらの検討からは、全身型MGの症状が最重症化またはほぼ最重症化した時期は、発症から6ヵ月以内が37%、発症6ヵ月~1年以内が29%であった3)。
多くの場合、MGは生涯にわたり慢性に経過する3)。発症早期に寛解に至った後、病勢が比較的安定して経過したとする報告7)もみられるものの、いったん寛解に至っても長期持続せず、再発することが少なくない8)。その要因の一つとして、長期投与が可能な経口薬のみでは寛解維持が困難なことが挙げられる9)。しかし、近年は治療法の進歩により、発症から5年以降は、重症度が軽減する傾向にあると報告されている3,8)。
MGにおける増悪およびクリーゼの発症要因
MG患者の多くは、経過中に少なくとも1回は症状の再燃を経験する8)。その誘因としては、感染症(主に上気道感染症)、治療薬の減量、重症型あるいは球麻痺型患者に対する高用量ステロイド投与、MG症状を悪化させる薬剤の使用、高温環境、精神的ストレスなどが知られている8)。一方、近年はクリーゼに至るような重篤な悪化は減少しており、本邦におけるクリーゼの発症頻度は9.1~14.8%と報告されている10,11)。クリーゼを発症しやすい背景因子としては、抗筋特異的受容体型チロシンキナーゼ抗体(抗MuSK抗体)陽性例、発症1年以内の症例、球症状を呈する症例、胸腺腫合併例、ならびに糖尿病、高血圧、虚血性心疾患などの併存疾患を有する症例が挙げられる12-15)。
MGの生命予後;クリーゼによる死亡の減少
近年は、クリーゼによる死亡が大幅に減少しており、その結果としてMG関連死はほとんどみられなくなっている16)。セルビアにおける1979~2008年大規模コホート研究(562例)では、MG関連死亡率は2%未満と報告されており17)、2000~2005年に米国の病院で診療を受けたMG患者5,502例の解析では、全体の死亡率は0.89%、MGクリーゼ発症例に限ると4.47%であった18)。健常者との比較では、MG患者の死亡率が高いとする報告と、差がないとする報告があり16)、現時点では明確な結論には至っていない。なお、MG患者の死亡に関連する因子としては、悪性腫瘍の合併、肺疾患、心疾患、脳血管障害、胸腺腫再発、糖尿病などが挙げられている17,19,20)。
MG患者の治療アウトカムとアンメット・メディカル・ニーズ
近年、免疫療法の普及により全身型MGの重症例や死亡例は減少し、生命予後は改善している9)。寛解率は20%未満にとどまるものの、「軽微な筋力低下は存在するが、日常生活には支障がない状態」である軽微症状(minimal
manifestations:MM)まで改善する頻度は50%以上とされている16)。Japan MG registry
study(2021年)では、全国13施設のMG患者1,710例を対象とした多施設共同横断研究として、治療後の病勢をMGFA Postintervention
Status(表1)21)で評価した結果、完全寛解4%、薬理学的寛解6%、MM
47%、改善31%、不変9%、増悪2%、再燃0.5%であった(表2)22)。このようにMGは完治が難しい一方で、適切な治療により病勢をコントロールできる例も増えてきている。
表1 MGFA Postintervention Status21)
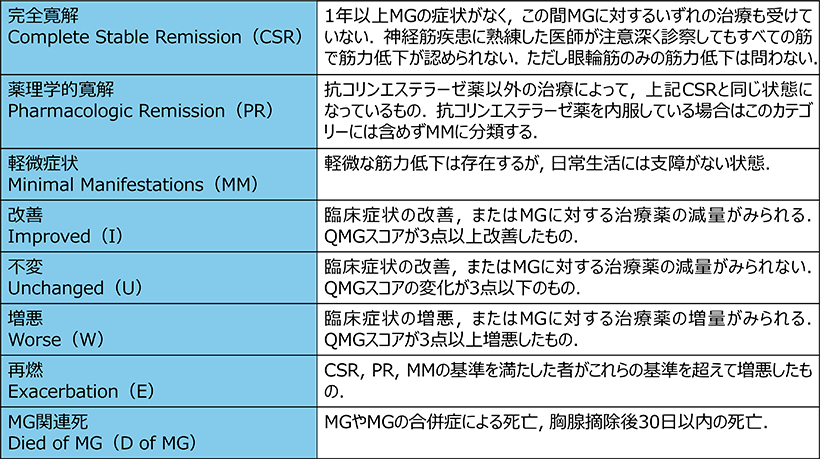 (Jaretzki A 3rd, et al. Neurology 2000; 55: 16-23. より作成)
(Jaretzki A 3rd, et al. Neurology 2000; 55: 16-23. より作成)
「日本神経学会 監修:重症筋無力症/ランバート・イートン筋無力症候群診療ガイドライン2022, p.28, 南江堂, 2022」より許諾を得て転載.
表2 MG患者の治療後の病勢(Japan MG registry study 2021年調査)22)
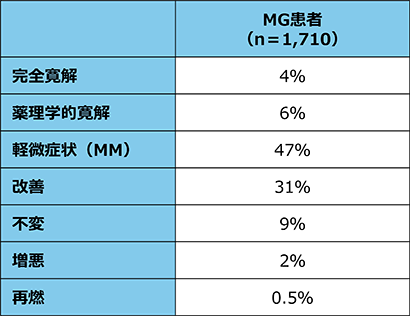
Suzuki S, et al.:Clin Exp Neuroimmunol. 2023;14:5-12.より改変
対象・方法:2021年に、全国13施設のMG症例1,710例を対象に多施設共同横断研究を実施し、MGFA Postintervention Status基準を用いて治療後の病勢を評価した。
一方で、依然MGのために日常生活に支障を感じている患者も少なからず認められる23)。2022年に日本人のMG患者を対象に実施したアンケート調査(有効回答452例)では、27.2%の患者が生活に満足できていないと回答している23)。多くは日常のさまざまな場面で支障を感じており、運動(73.7%)、仕事(68.0%;該当しない、無回答を除く)、趣味(60.4%)、旅行(60.0%)、友人と外出(59.7%)において割合が高かった(図1)23)。さらに、約50%は入院によって仕事に支障をきたすことがあると回答している23)。
こうした結果は、MG治療のアンメット・メディカル・ニーズの存在を示唆している23)。特に、抗MuSK抗体陽性患者群、および抗AChR抗体と抗MuSK抗体がともに陰性のダブルセロネガティブの患者群では、「生活に満足できていない」と回答した割合が、抗AChR抗体陽性患者群より高く、これらの患者における新たな治療法が期待される23)。
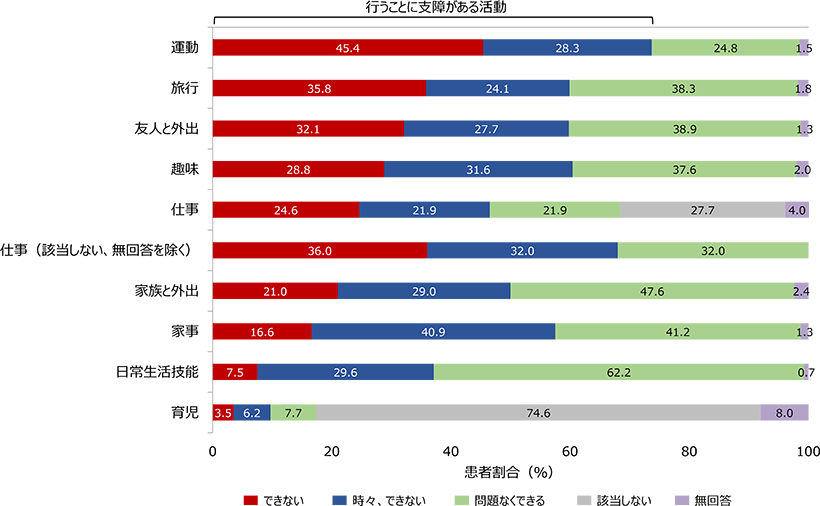 図1 日常的活動の実施状況
対象・方法:重症筋無力症友の会および筋無力症患者会が、日本でMGと診断され定期的に外来治療を受けているMG患者を募集し、2022年4月20日~5月8日に464例を対象にオンラインあるいは郵送でアンケート調査を実施した(有効回答452例)。
リミテーション:本研究は日本国内の患者を対象としており、他国や異なる人種・民族への一般化には限界がある。患者会の会員を中心に調査を実施したため、疾患管理や調査参加に積極的な患者に偏っている可能性がある。参加者には女性や高齢者、併存疾患を有する者が多く、うつ病などの心理的要因を評価しておらず、結果に影響を与えた可能性がある。検証されていないクローズド式
(提示された選択肢から回答を選ぶ形式) の質問票を用いた。診断および治療情報は患者の自己申告に基づいて収集した。
図1 日常的活動の実施状況
対象・方法:重症筋無力症友の会および筋無力症患者会が、日本でMGと診断され定期的に外来治療を受けているMG患者を募集し、2022年4月20日~5月8日に464例を対象にオンラインあるいは郵送でアンケート調査を実施した(有効回答452例)。
リミテーション:本研究は日本国内の患者を対象としており、他国や異なる人種・民族への一般化には限界がある。患者会の会員を中心に調査を実施したため、疾患管理や調査参加に積極的な患者に偏っている可能性がある。参加者には女性や高齢者、併存疾患を有する者が多く、うつ病などの心理的要因を評価しておらず、結果に影響を与えた可能性がある。検証されていないクローズド式
(提示された選択肢から回答を選ぶ形式) の質問票を用いた。診断および治療情報は患者の自己申告に基づいて収集した。
Kawaguchi N, et al.:Neurol Ther. 2024;13(4):1099-1113.
MGの予後改善を目指して
MGはかつて呼吸不全やクリーゼによる死亡が問題であったが、現在は治療の進歩により、社会生活を維持できるまでに病勢をコントロールすることが可能な患者も増えている。一方で、完全寛解に至る割合は依然として低く、長期的な診療では症状の再燃リスクに加えて、ステロイドや免疫治療薬などの長期投与に伴う感染症、糖尿病、骨折といった治療関連有害事象にも十分配慮した包括的な管理が重要である。
特に高齢発症例や胸腺腫関連例では、感染症や併存疾患が生命予後に影響しやすく、包括的な管理が求められる。これらの患者における予後への影響因子として、高齢患者では肺炎や骨折、QOLの低下が報告されている24,25)。胸腺腫関連例では、心筋炎や免疫不全の合併26)に加え、56歳以上、胸腺腫摘除後の顕微鏡的残存または肉眼的残存、正岡の分類Ⅲ以上、WHO分類B1~3などが予後不良因子として報告されている27)。
今後必要とされる多面的アプローチ
MG治療において、実生活に不満や制限を感じている患者が依然として少なくない23)。特にMG治療に不満のある患者では、医師との信頼関係や治療選択における情報共有について、十分でないと感じるケースも少なくないことが報告されており17)、医師と患者が対話を通じて共に治療方針を決定する共同意思決定(シェアード・ディシジョン・メイキング:SDM)を、今後さらに意識する必要があると考えられる。また、MG患者の多くが「症状による日常生活上の支障がない状態」を治療目標として挙げていることからも23)、その達成に向けて、通院負担を抑えつつ継続可能な外来ベースの治療選択肢の拡充や、在宅での自己管理を支援する体制の強化が求められる。
さらに、新たな分子標的治療薬や次世代の抗体製剤の活用、またバイオマーカーを基盤とした個別化医療の実現によって、より安定した長期予後の確保が期待される。また、高齢患者を含む多様な症例のさらなる予後改善と患者満足度の向上を目指すには、包括的管理や治療法の拡充などの医療の強化とともに、就労支援や社会的理解の促進など社会的支援も含めた多面的なアプローチが重要となろう。
参考文献
- Benatar M, Kaminski H:Cochrane Database Syst Rev. 2006;(2):CD005081.
- Benatar M, et al.:Neurology. 2007;68(24):2144-2149.
- Grob D, et al.:Muscle Nerve. 2008;37(2):141-149.
- Fang CEH, et al.:Neurology. 2023;101(16):e1594-e1605.
- Hendricks TM, et al.:Am J Ophthalmol. 2019;205:99-105.
- Bever CT Jr, et al.:Ann Neurol. 1983;14(5):516-519.
- Shibuya M, et al.:Tohoku J Exp Med. 2024;262(1):29-31.
- Hehir MK, Silvestri NJ:Neurol Clin. 2018;36(2):253-260.
- 日本神経学会監修:重症筋無力症/ランバート・イートン筋無力症候群診療ガイドライン2022. 2022, 南江堂, p.50-53.
- Murai H, et al.:J Neurol Sci. 2011;305(1-2):97-102.
- 長根百合子:臨床神経学. 2013;53(11):1299-1302.
- Khadilkar SV, et al.:Neurol India. 2014; 62(5):492-497.
- Kalita J, et al.:Neurol Sci. 2014;35(7):1109-1114.
- Lacomis D:Neurocrit Care. 2005;3(3):189-194.
- Sanders DB, et al.:Autoimmunity. 2010;43(5-6):428-435.
- 日本神経学会監修:重症筋無力症/ランバート・イートン筋無力症候群診療ガイドライン2022. 2022, 南江堂, p.41-43.
- Basta I, et al.:Muscle Nerve. 2018;58(5):708-712.
- Alshekhlee A, et al.:Neurology. 2009;72(18):1548-1554.
- Liu C, et al.:Neurol India. 2017;65(3):518-524.
- Owe JF, et al.:J Neurol Neurosurg Psychiatry. 2006;77(2):203-207.
- 日本神経学会監修:重症筋無力症/ランバート・イートン筋無力症候群診療ガイドライン2022. 2022, 南江堂, p.28.
- Suzuki S, et al.:Clin Exp Neuroimmunol. 2023;14:5-12.
- Kawaguchi N, et al.:Neurol Ther. 2024;13(4):1099-1113.
- Alkhawajah NM, Oger J:Drugs Aging. 2015;32(9):689-697.
- Tiamkao S, et al.:Int J Gen Med. 2017;10:131-135.
- Suzuki S, et al.:J Neurol Neurosurg Psychiatry. 2013;84(9):989-994.
- Nakajima J, et al.:Eur J Cardiothorac Surg. 2016;49(5):1510-1515.



 (Jaretzki A 3rd, et al. Neurology 2000; 55: 16-23. より作成)
(Jaretzki A 3rd, et al. Neurology 2000; 55: 16-23. より作成)
 図1 日常的活動の実施状況
対象・方法:重症筋無力症友の会および筋無力症患者会が、日本でMGと診断され定期的に外来治療を受けているMG患者を募集し、2022年4月20日~5月8日に464例を対象にオンラインあるいは郵送でアンケート調査を実施した(有効回答452例)。
リミテーション:本研究は日本国内の患者を対象としており、他国や異なる人種・民族への一般化には限界がある。患者会の会員を中心に調査を実施したため、疾患管理や調査参加に積極的な患者に偏っている可能性がある。参加者には女性や高齢者、併存疾患を有する者が多く、うつ病などの心理的要因を評価しておらず、結果に影響を与えた可能性がある。検証されていないクローズド式
(提示された選択肢から回答を選ぶ形式) の質問票を用いた。診断および治療情報は患者の自己申告に基づいて収集した。
図1 日常的活動の実施状況
対象・方法:重症筋無力症友の会および筋無力症患者会が、日本でMGと診断され定期的に外来治療を受けているMG患者を募集し、2022年4月20日~5月8日に464例を対象にオンラインあるいは郵送でアンケート調査を実施した(有効回答452例)。
リミテーション:本研究は日本国内の患者を対象としており、他国や異なる人種・民族への一般化には限界がある。患者会の会員を中心に調査を実施したため、疾患管理や調査参加に積極的な患者に偏っている可能性がある。参加者には女性や高齢者、併存疾患を有する者が多く、うつ病などの心理的要因を評価しておらず、結果に影響を与えた可能性がある。検証されていないクローズド式
(提示された選択肢から回答を選ぶ形式) の質問票を用いた。診断および治療情報は患者の自己申告に基づいて収集した。

